聚焦2025年版中国药典丨各国及地区药典标准体系总体架构比较
- 2025-03-24 11:31
- 作者:
- 来源:《中、美、欧、日药典体系架构的比较》,中国药品标准,2024,25(3),209
药品标准体系的完善程度对药品安全的保障起到举足轻重的作用。药典是药品标准体系的核心,是一个国家或地区记载药品标准、规格的法典,一般由官方机构或由该国或地区法律授权的组织负责制定。近年来,随着科技的飞速发展,以及为加深使用者对监管目标的理解,许多国家和地区的药典标准体系均在不断完善。本文针对2020年版《中国药典》《美国药典-国家处方集》(USP/NF)现行版、《欧洲药典》(EP) 11.0版、《日本药局方》(JP)第18版、《英国药典》(BP)2023版、《国际药典》(IP)第11版标准体系,对比各国及地区药典标准体系总体架构如下:
从收载范围上看,由于各国及地区药品监管法规存在差异,以及受药典外标准的影响,除药品标准外,USP/NF 收载了膳食补充剂标准;EP 收载了顺势疗法制剂标准;BP 收载了外科手术用材料、兽药标准。
从标准配套信息收载上看,JP、BP、IP 均收载了部分药品的红外光谱图或紫外光谱图;USP/NF 提供了有关色谱柱信息等更多资源。
从标准类型收载上看,USP/NF收载了新型标准“启动文章”,阐述新的、前沿的标准制定意向或计划,提前介绍下一步标准增修订工作,以便利益相关方提前知晓和参与。
从收载数量上看,不同专业领域的各类型标准的数量不同。
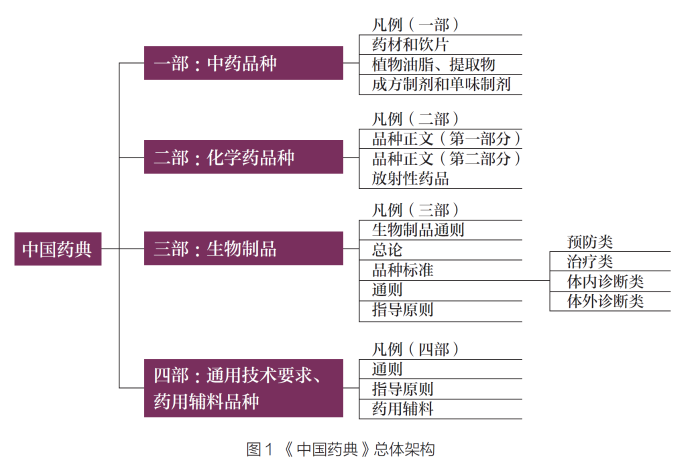
《中国药典》
收载中药各论标准最多。除《中国药典》外,我国还存在其他局(部)颁等标品种标准。
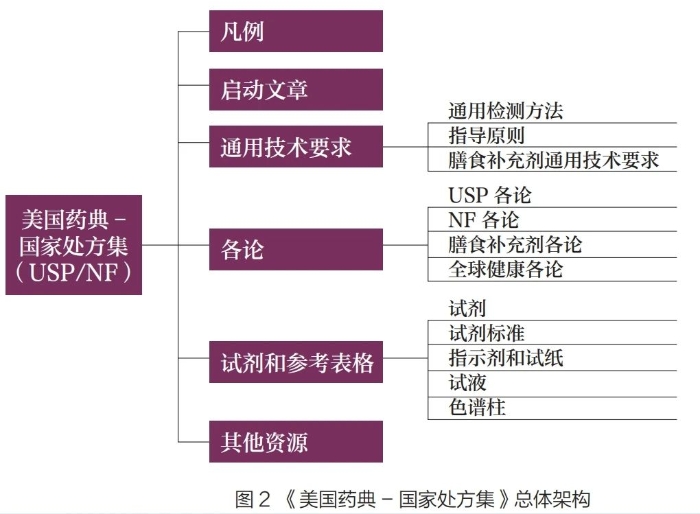
USP/NF
收载的化学药原料药、辅料和制剂各论标准最多,但收载的生物制品标准较少,这是由于美国《联邦法规汇编》(CFR)第21篇“食品与药品”600~660部,以及美国食品药品管理局(FDA)发布的相关指南涵盖了生物制品的质量控制和生产。2010年以前,USP/NF 收载了比现在更多的生物制品品种标准,但在2010年左右被删除,原因包括:缺乏质量信息,不再在美国销售,只提到了检测项目但没有提供方法,许可证被吊销,不再以同样的方式生产,或者生产被纳入FDA 关于生物制品的法规范畴等。USP/NF收载的通用技术要求标准最多。
EP
只收载了少量制剂标准,制剂产品的质量需要符合各成员国药典或药品管理当局批准的质量标准要求。

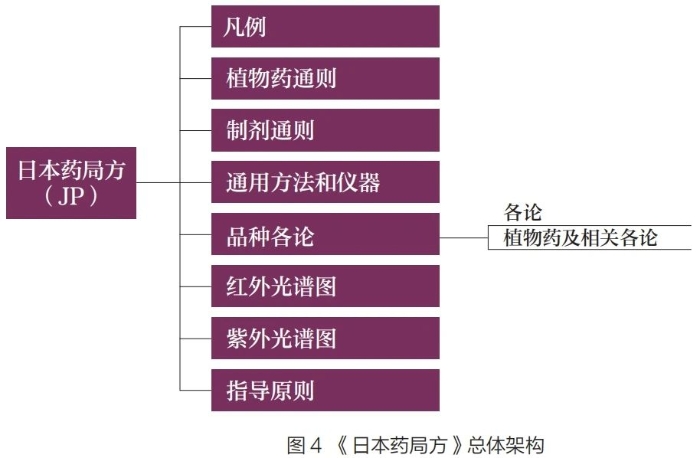
JP
收载的各类型标准均较少,这是因为日本还存在大量JP 外的法定标准,如日本生物制品最低要求、日本放射性药品标准、日本药局方外标准、日本药局方外生药标准、日本药用辅料标准等。
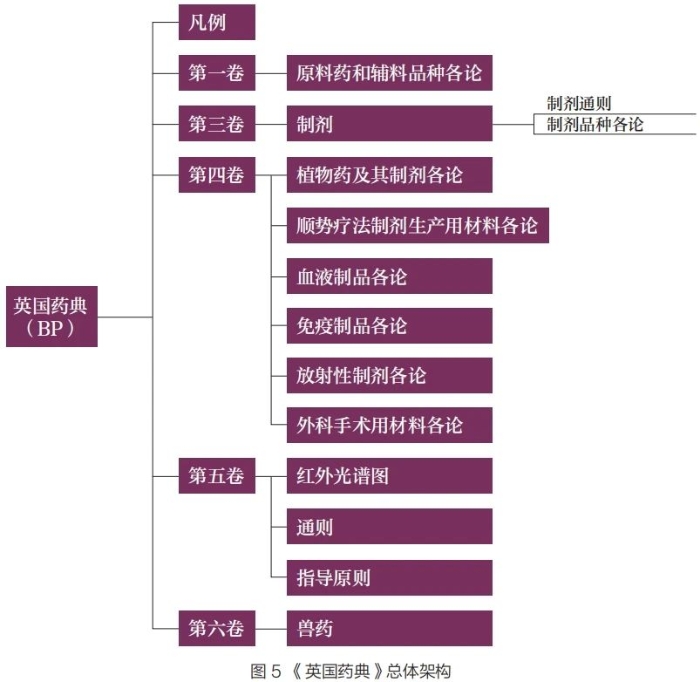
BP
根据与欧洲药品质量管理局(EDQM)签订的合作协议,BP复制了EP的标准,还收载了BP特有的标准。
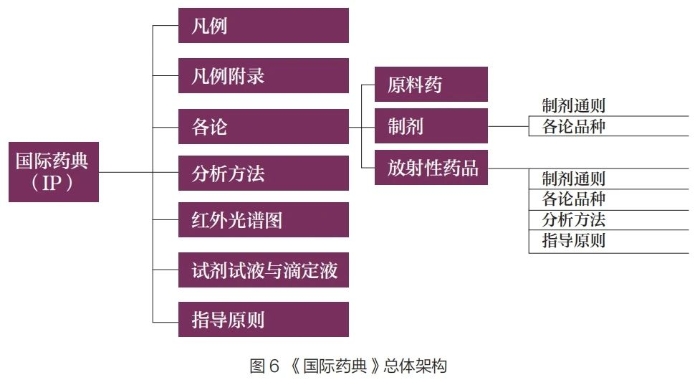
IP
主要收载化学药品和辅料标准,对于放射性药品的通用技术要求收载较多。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:常靖婕)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐
-

-

互联网新闻信息服务许可证10120170033
网络出版服务许可证(京)字082号
©京公网安备 11010802023089号 京ICP备17013160号-1
《中国医药报》社有限公司 中国食品药品网版权所有










