每周医药看点(7月28日—8月3日)
- 2025-08-08 14:23
- 作者:刘鹤
- 来源:中国食品药品网
中国食品药品网讯 国家药监局等三部门联合发布《药用类麻醉药品目录(2025年版)》和《药用类精神药品目录(2025年版)》;国家药监局公布药品说明书适老化及无障碍改革试点名单(第五批)……7月28日—8月3日,医药行业的这些动态值得关注。
行业政策及药监动态
1.国家药监局、公安部、国家卫生健康委联合发布实施《药用类麻醉药品目录(2025年版)》和《药用类精神药品目录(2025年版)》。此外,三部门还联合发布了最新版《非药用类麻醉药品和精神药品目录》,原《非药用类麻醉药品和精神药品管制品种增补目录》废止。
2.国家药监局公布药品说明书适老化及无障碍改革试点名单(第五批),包含华润赛科药业有限责任公司的维格列汀片等222个药品。
3.国家药监局综合司发布通知,2025年“全国药品安全宣传周”活动时间确定为9月1日—7日,主题为“药品安全 监管为民”。
4.国家药监局药品审评中心(CDE)发布《模型引导的罕见疾病药物研发技术指导原则》《罕见疾病药物临床药理学研究技术指导原则》《发酵或半合成化学仿制药抗生素有关物质限度制定指导原则》《药物暴露-效应关系研究技术指导原则》,为相关药物研究提供指导。
5.CDE就《嗜酸性粒细胞性食管炎治疗药物临床试验技术指导原则(征求意见稿)》公开征求意见。制定该指导原则,旨在为嗜酸性粒细胞性食管炎治疗药物的研发提供技术指导。
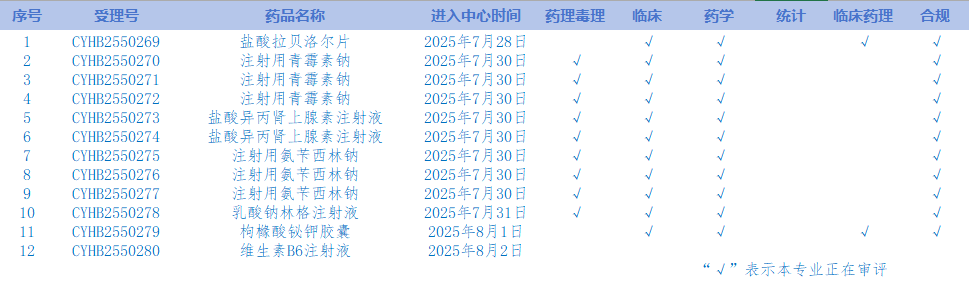
6.CDE网站公示12个仿制药质量和疗效一致性评价任务,涉及盐酸拉贝洛尔片等品种。
产品研发上市信息
1.国家药监局发布5期药品批准证明文件送达信息,共包括415个受理号,涉及利培酮口溶膜等品种。
2.CDE承办受理80个新药上市申请,包括益气升脉颗粒等。
3.康宁杰瑞宣布,公司自主研发的HER2双抗偶联药物JSKN003已获得美国食品药品管理局(FDA)批准开展铂耐药卵巢癌Ⅱ期临床研究。
4.优替济生宣布,公司自主研发的LACOStim自体MSLN CAR-T细胞疗法(UCLM805)的新药临床试验(IND)申请获美国FDA批准,用于间皮素阳性的成人晚期实体瘤患者。
医药企业观察
1.恒瑞医药宣布与葛兰素史克达成合作协议,双方将共同开发至多12款创新药物。协议包含一款PDE3/4抑制剂(HRS-9821)的授权许可,该产品目前正处于慢性阻塞性肺疾病治疗的临床开发阶段;其余11个项目将由恒瑞医药主导研发,最晚至Ⅰ期临床试验结束,葛兰素史克可行使优先选择权。根据协议,葛兰素史克将向恒瑞医药支付总计5亿美元的首付款。
2.泽安生物宣布与礼来达成战略合作,旨在针对特定靶点开发全新的髓系细胞衔接器药物,用于治疗未满足需求的自身免疫性疾病。根据协议,泽安生物将获得数千万美元首付款,并得到礼来的股权投资。此外,在药物研发的临床前、临床、监管审批和商业化等阶段,泽安生物还有资格收取潜在里程碑付款。
3.博瑞医药宣布,与华润三九达成合作研发协议。根据协议,博瑞医药将与华润三九在合作区域内就BGM0504注射液共同进行后续开发,并推进商业化进程。BGM0504注射液是一款GLP-1和GIP受体双重激动剂,拟用于治疗2型糖尿病和肥胖症。
4.健民集团宣布,与湖北福人药业达成战略合作。双方将以葡萄糖酸钙锌口服溶液为核心合作纽带,开启在儿科健康领域的深度协作。
药品集中采购
1.安徽省医药价格和集中采购中心发布通知,开始开展部分单抗类生物制剂信息填报收集工作,凡生产《部分单抗类生物制剂信息收集汇总表》内品规药品的企业均可以参与信息填报,其中包含阿达木单抗等品种。
2.河南省公共资源交易中心公示部分药品价格风险处置结果,涉及湖南千金湘江药业股份有限公司拉米夫定片等品种。公示时间为2025年7月28日—30日。(刘鹤整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:周雨同)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐