每周医药看点(9月30日—10月13日)
- 2024-10-15 16:34
- 作者:张可欣
- 来源:中国食品药品网
中国食品药品网讯 市场监管总局发布《医药企业防范商业贿赂风险合规指引(征求意见稿)》;国家药监局发布境内生产药品再注册申报程序和申报资料要求;国家药监局药品审评中心发布《抗肿瘤药物临床试验中SUSAR分析与处理技术指导原则》……9月30日—10月13日,医药行业的这些动态值得关注。
行业·政策动态
1.市场监管总局发布《医药企业防范商业贿赂风险合规指引(征求意见稿)》(以下简称《征求意见稿》)并公开征求意见。《征求意见稿》涉及学术拜访交流、临床研究、零售终端销售等9个场景的医药领域商业贿赂风险点,为医药企业防范商业贿赂风险合规管理提供具体、可操作的指导建议。意见反馈截止日期为10月20日。
2.国家药监局发布境内生产药品再注册申报程序和申报资料要求,自2025年1月1日起施行。
3.国家药监局发布《关于对药品、医疗器械质量安全内部举报人举报实施奖励的公告(征求意见稿)》(以下简称《征求意见稿》)并公开征求意见。根据《征求意见稿》,药品、医疗器械研制、生产、经营企业和使用单位,网络药品、医疗器械交易第三方平台提供者以及其他组织的内部员工、相关知情人,向药监部门举报药品、医疗器械质量安全重大违法行为的,适用本公告。对媒体记者等相关知情人举报实施奖励可参照执行。
4.国家药监局发布化学仿制药参比制剂目录(第八十三批),涉及甲磺酸氟马替尼片等药品。
5.国家药监局发布公告,对含美洛西林钠注射剂[包括注射用美洛西林钠、注射用美洛西林钠舒巴坦钠、注射用美洛西林钠舒巴坦钠(4:1)],阿魏酸哌嗪口服制剂(包括阿魏酸哌嗪片、阿魏酸哌嗪分散片和阿魏酸哌嗪胶囊),以及葡醛酸钠注射制剂(包括葡醛酸钠注射液、注射用葡醛酸钠、葡醛酸钠氯化钠注射液)说明书内容进行统一修订。
6.国家药监局发布公告,对通便灵胶囊说明书中的【警示语】、【不良反应】、【禁忌】和【注意事项】进行统一修订。
7.国家药监局药品审评中心(CDE)发布《抗肿瘤药物临床试验中SUSAR分析与处理技术指导原则》,加强临床试验中SUSAR(可疑且非预期严重不良反应)信息的风险评估,提升SUSAR信息的发现、识别和风险处理。
8.CDE就《模型引导的罕见病药物研发技术指导原则(征求意见稿)》《罕见病药物临床药理学研究技术指导原则(征求意见稿)》公开征求意见。征求意见时限均为自发布之日起1个月。
9.CDE网站公示12个仿制药一致性评价任务,涉及盐酸曲唑酮片等品种(截至10月13日)。
产品研发·上市信息
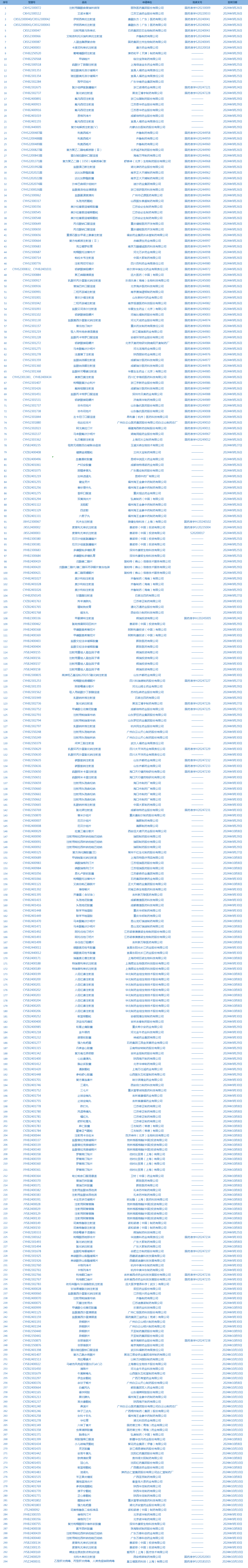
1.国家药监局发布5期药品批准证明文件送达信息,共包括294个受理号,涉及丽珠医药集团股份有限公司等企业(截至10月13日)。
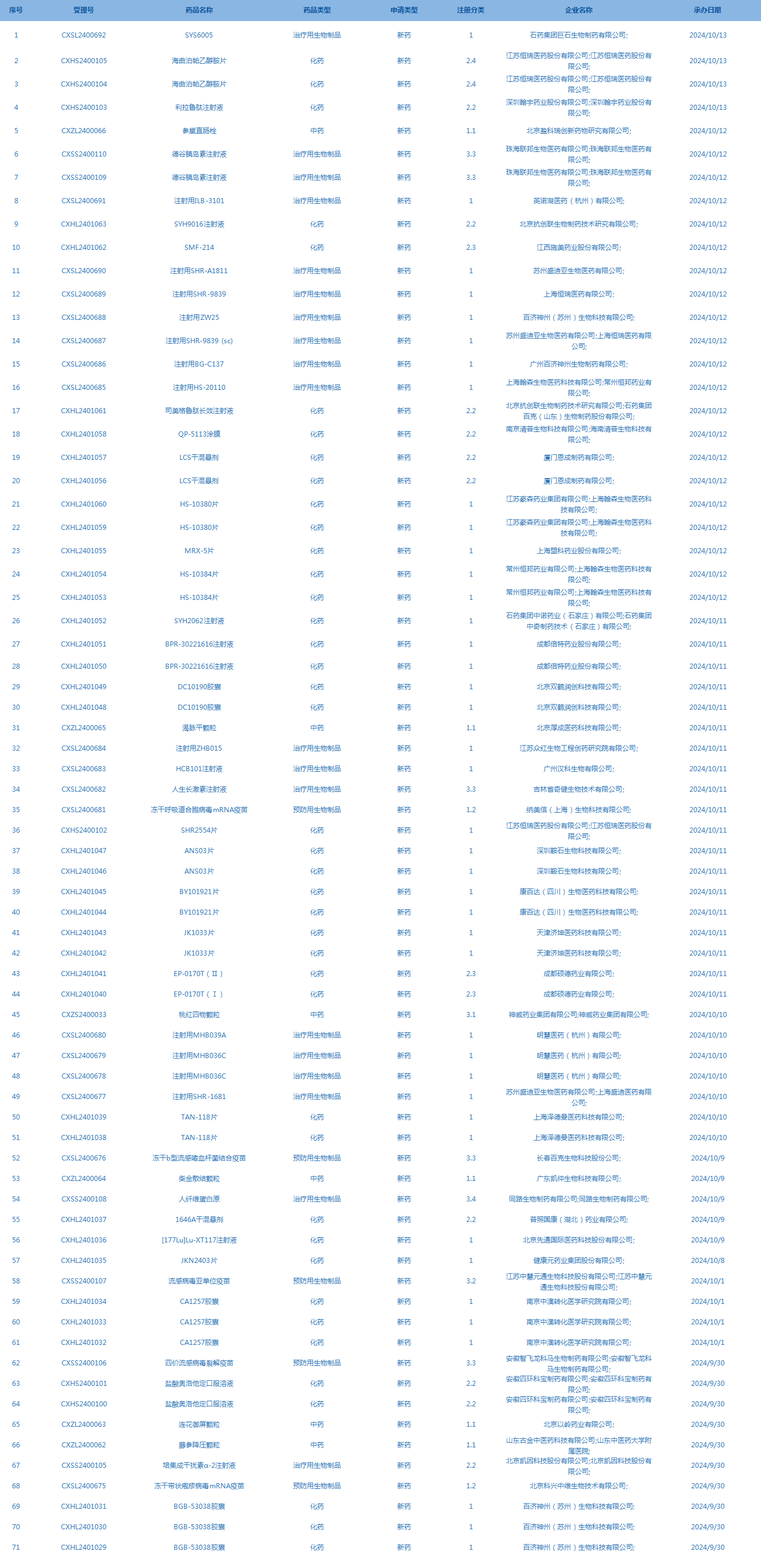
2.CDE承办受理71个新药上市申请,包括海曲泊帕乙醇胺片等(截至10月13日)。
3.亿帆医药发布公告称,全资子公司SciGen Pte. Ltd.近日收到新加坡卫生科学局核准签发的中成药注册批文,批准公司独家医保产品皮敏消胶囊在新加坡上市销售。
4.普洛药业发布公告称,其全资子公司浙江巨泰药业有限公司的产品盐酸金刚烷胺片获得美国食品药品管理局(以下简称美国FDA)上市批准。
5.沃森生物发布公告称,其子公司玉溪泽润生物技术有限公司生产的双价人乳头瘤病毒疫苗(毕赤酵母)于近日收到印度尼西亚食品与药品管理局签发的《产品上市许可证》,双价HPV疫苗预灌封和西林瓶两个品规均获得了印度尼西亚上市许可。
6.恒瑞医药发布公告称,公司向美国FDA申报的注射用紫杉醇(白蛋白结合型)ANDA(简略新药申请)已获得批准。
7.百济神州称,公司产品替雷利珠单抗在美国正式商业化上市,用于治疗既往接受过系统化疗(不含PD-1/L1抑制剂)后不可切除或转移性食管鳞状细胞癌(ESCC)的成人患者。
医药企业观察
1.嘉和生物发布公告,宣布与亿腾医药订立合并协议。嘉和生物将通过合并方式收购亿腾医药,合并后的新公司名称预计将改为亿腾嘉和。
2.强生公司下属杨森生物技术公司与晶泰科技下属部门Ailux Biologics签署大分子药物发现AI平台授权协议。根据协议,晶泰科技商业授权杨森生物技术公司及其附属公司使用Ailux Biologics自主开发的XtalFold AI平台进行大分子药物的发现和工程化设计。
3.石药集团发布公告称,已与阿斯利康签订独家授权协议,同意授予阿斯利康在全球范围内开发、制造及商业化脂蛋白(a)(Lipoprotein(a),Lp(a))抑制剂YS2302018,以及后续开发的由该化合物组成或含有该化合物的任何药品或生物制品的独家授权。石药集团将收取1亿美元的预付款,并有权收取最高3.7亿美元的潜在开发里程碑付款及最高15.5亿美元的潜在销售里程碑付款,以及根据相关产品的年度销售净额计算的分层销售提成。
4.成都先导与成都盛世君联生物技术有限公司宣布达成战略合作协议,将深度融合双方拥有的全球领先的万亿级DNA编码化合物库(DEL)、完整的小核酸药物发现生产平台和三千亿级生物药物分子库,共同对外提供抗体—寡核苷酸偶联药物的研发服务。
5.多瑞医药发布公告称,公司与前沿生物、上海前沿建瓴生物科技有限公司(以下简称上海建瓴)签署了《投资意向协议》,拟通过股权受让的方式投资上海建瓴,目标持股比例70%。公司已支付投资意向金1,000.00万元。本次交易完成后,上海建瓴纳入公司的合并报表范围。
6.百奥泰发布公告称,与GedeonRichter Plc.(以下简称吉瑞医药)就BAT2206(乌司奴单抗)注射液签署授权许可及生产、供货和商业化协议,将BAT2206(乌司奴单抗)注射液在欧盟、英国、瑞士、澳大利亚以及其他部分欧洲国家市场的独占的产品商业化权益有偿许可给吉瑞医药。协议生效后,吉瑞医药将向百奥泰一次性支付850万美元首付款,且在百奥泰达到相应的里程碑事件后向其支付累计不超过1.015亿美元的里程碑款。
7.礼来中国宣布将投资约15亿元人民币用于其苏州工厂的产能升级,扩大2型糖尿病和肥胖创新药物的生产规模,以满足患者需求,并支持未来管线产品的生产。
8.睿健医药宣布完成超亿元B轮融资。本轮融资由策源资本和国生资本联合领投。融资资金将用于加速推进公司帕金森病治疗产品NouvNeu001/NouvNeu003,以及眼科治疗产品NouvSight001的中美临床研究,加强多款创新管线的研发推进和临床能力搭建等。
9.康方生物宣布,公司已经完成新一轮股票配售,成功融资约19.42亿港元。本次股票配售获得了国际投资机构的广泛认可,最终实际认购的投资机构主要为国际性的长线基金和专业医疗基金。据悉,本次融资金额的70%,将用于加速康方生物自主研发新药在全球范围内的临床开发。
药品集中采购
1.陕西省医保局印发《陕西省开展集采药品“三进”行动实施方案》的通知,将在全省开展集采药品进零售药店(包括连锁/单体药店)、民营医疗机构、村卫生室(包括社区卫生服务中心/站)行动,其中涉及295个通用名、1110个品规药品。
2.甘肃省医疗保障局发布《甘肃省第六批药品集中带量采购公告(第1号)》,拟开展甘肃省第六批药品集采工作(带量联动专项)。本次拟集采药品遴选的基本原则是其他省份已集采且过评企业(含原研和参比制剂)数4家及以下的中成药和化学药品种(按大类剂型合并,不区分酸根碱基)。本次拟纳入集采的品种共332个,其中化学药187个,中成药145个。
3.湖北省医疗保障局发布《关于调整部分挂网药品价格信息的通知》,调整挂网价的已挂网药品共110个,涉及64家企业86个通用名药品。自2024年10月11日起执行。(本报记者张可欣整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:周雨同)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐