2月份美国Clinicaltrial数据库临床试验数据显示——我国三家企业进入新开临床试验数量排名前十
- 2025-04-03 09:29
- 作者:陈宇哲
- 来源:中国医药报
根据美国Clinicaltrial数据库数据,2025年2月份,全球新增由企业资本主导的临床试验总数为652项,新开临床试验数量较1月份下降7.52%。单月新增临床试验数量显著高于去年同期水平,上升19.85%。值得注意的是,我国有3家企业进入新开临床试验数量排名前十,分别为山东盛迪医药、神州细胞和微康益生菌。
新开临床试验整体情况
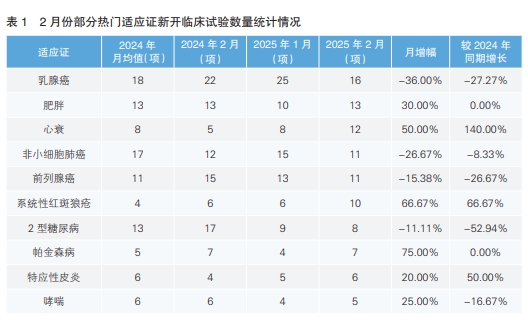
从2月份新增临床试验热门适应证领域来看,乳腺癌为最热门的研发领域,试验数量为16项,环比下降36.00%,相较于去年同期数量下降27.27%。其次为肥胖,新开临床试验数量环比上升30.00%,与去年同期数量持平。值得注意的是,2月份新增临床试验数量上升幅度最高的热门适应证为帕金森病,由1月份的4项上升为7项,上升幅度为75%。除此之外,相较于去年同期,上升幅度最大的适应证为心衰,由5项上升为12项,增幅为140%。(详见表1)
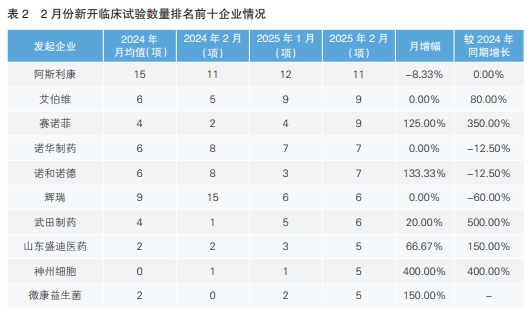
对新增临床试验的发起企业进行统计后发现,2月份发起临床试验最多的企业为阿斯利康,数量相较于1月份下降了8.33%,但与去年同期持平。其次为艾伯维,数量与1月份持平,较去年同期增长80.00%。与1月份相比,新增临床试验数量增幅最大的企业为我国的神州细胞,环比上升了4倍。相较于去年同期,数量上升幅度最大的为武田制药,上涨了5倍。(详见表2)
对临床试验的申请国家和地区进行统计后发现,2月份美国仍为临床试验开展最为主要的国家,新开展临床试验218项,数量环比下降了1.80%。其次是中国,新开设临床试验数量为80项,数量环比上升了1.27%。2月份新开临床试验数量月增长幅度最大的国家为荷兰,由6项增长为7项,增长幅度为16.67%。
我国三家企业新增5项临床试验
2月份,我国的山东盛迪医药、神州细胞和微康益生菌均进入新开临床试验数量排名前十的企业榜单。这3家企业新开设临床试验均为5项。
山东盛迪医药2月份新增临床试验包括3项Ⅱ期临床试验和两项Ⅰ期临床试验。
3项Ⅱ期临床试验的药物分别为HRS-7535(NCT06820099),适应证为成人肥胖伴心力衰竭伴射血分数保留;HRS-5346(NCT06816264),适应证为脂蛋白紊乱的治疗;HRS-1893(NCT06816251),适应证为非梗阻性肥厚型心肌病。
公开数据显示,HRS-7535是一种新型口服小分子GLP-1RA。临床前研究发现,在无严格限食的情况下,HRS-7535可明显改善葡萄糖耐量,促进胰岛素分泌,减少摄食量。HRS-5346是一种口服小分子脂蛋白(a)[也称Lp(a)]抑制剂。Lp(a)是一类独特的脂蛋白,含有低密度脂蛋白样颗粒,具有促动脉粥样硬化、促炎、促钙化等作用。高Lp(a)是动脉粥样硬化性心血管疾病的独立危险因素,也是主动脉瓣狭窄的危险因素。因此,靶向Lp(a)的降脂疗法是心血管疾病防治的重要突破点之一。HRS-1893可通过特殊机制抑制心肌过度收缩。据悉,该药是国内第一个使用心脏器官芯片数据获批I ND的新药。
两项Ⅰ期临床试验的药品分别为[14C] HRS-7535(NCT06819488),适应证为2型糖尿病;HRS-2129(NCT06780267),适应证为骨科术后疼痛。
神州细胞新增的5项临床试验均处于Ⅰ/Ⅱ期临床试验阶段,其中两项为药品,两项为疫苗,一项为生物疗法。
两款药物分别为SCTT11(NCT06769984)适应证为甲状腺眼病,以及SCT520FF(NCT06672536),适应证为新生血管性黄斑变性。公开资料显示,这两款药品均为单克隆抗体。两款疫苗中,SCTV04C(NCT06801509)的适应证为带状疱疹;另一款疫苗SCTV02(NCT06754605),适应证为呼吸道合胞病毒。生物疗法为SCTB35(NCT06841042),适应证为系统性红斑狼疮。根据公开资料,SCTB35是神州细胞开发的CD20/CD3双抗。
微康益生菌的5项临床试验,试验对象均为膳食补充剂。
(数据来源于美国Clinicaltrial数据库,统计时间为2025年3月5日)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:张可欣)
分享至
右键点击另存二维码!
-
为你推荐