每周医药看点(9月1日—7日)
- 2025-09-11 09:54
- 作者:
- 来源:中国医药报
2025年“全国药品安全宣传周”启动仪式9月1日在京举办;国家药监局发布《仿制药参比制剂目录(第九十五批)》,包括贝组替凡片等品种……9月1日—7日,医药行业的这些动态值得关注。
行业政策及药监动态
1.9月1日,2025年“全国药品安全宣传周”启动仪式在京举办。本次宣传周的主题为“药品安全 监管为民”,活动时间为9月1日—7日。各级药监部门通过组织丰富多彩的宣传活动,进一步增强全民药品安全意识,营造良好共治氛围。
2.国家药监局发布《仿制药参比制剂目录(第九十五批)》,包括贝组替凡片等品种。
3.国家药监局食品药品审核查验中心发布《药物临床试验生物样品分析实验室管理指南》,旨在提高药物临床试验生物样品分析实验室的管理水平,确保生物样品分析数据的质量。
4.国家药监局药品审评中心(CDE)发布通知,将北京康辰药业股份有限公司的KC1036片纳入儿童抗肿瘤药物研发鼓励试点计划(星光计划),拟开发的儿童适应证为尤文肉瘤。
5.CDE就《针对泛肿瘤的抗肿瘤药物临床研发技术指导原则(征求意见稿)》公开征求意见。制定该指导原则,旨在阐述当前针对泛肿瘤药物临床研发中相关技术问题的考虑。
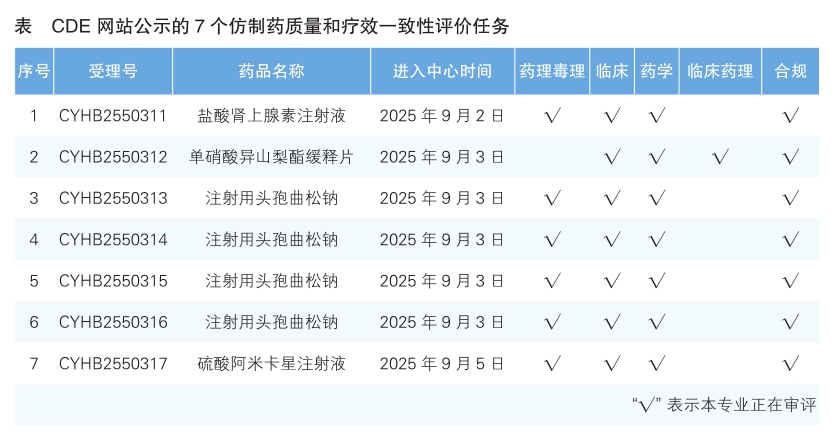
6.CDE网站公示7个仿制药质量和疗效一致性评价任务(详见表),涉及盐酸肾上腺素注射液等品种。
产品研发上市信息
1.国家药监局发布4期药品批准证明文件送达信息,共包括300个受理号,涉及江苏恒瑞医药股份有限公司等企业。
2.CDE承办受理78个新药上市申请,包括小儿六味湿疹凝胶等。
3.复宏汉霖宣布,其60mg/mL、120mg/1.7mL两种规格的地舒单抗注射液的生物制品许可申请获美国食品药品管理局(FDA)批准。
医药企业观察
1.恒瑞医药宣布,与美国生物科技公司 Braveheart Bio达成独家许可协议,将自主研发的心肌肌球蛋白小分子抑制剂HRS-1893在除中国以外的全球范围内开发、生产和商业化的独家权利有偿许可给Braveheart Bio。根据协议,Braveheart Bio将向恒瑞医药支付6500万美元首付款和完成技术转移后的1000万美元近期里程碑款;恒瑞医药还将收取最高可达10.13亿美元的与临床开发和销售相关的里程碑付款,以及相应的销售提成。
2.百奥赛图宣布,与德国默克达成协议,共同推进开发应用于核酸药物的抗体偶联脂质递送解决方案。根据协议,百奥赛图将提供基于其RenMice平台自主开发的全人抗体,由默克评估将其用于抗体偶联LNP制剂服务的可行性。默克被授予获取选中抗体资产权益的独家选择权,百奥赛图有权获得相应的费用付款及销售分成和再许可分成。
3.舶望制药宣布,与诺华达成一项战略合作协议。根据协议,舶望制药授予诺华两款处于早研阶段分子的中国以外权益的选择权;针对另一款处于临床前研究阶段的siRNA候选药物,舶望制药授予诺华独家中国地区以外许可,并包含在美国和中国分享损益的互惠选择权。舶望制药将获得1.6亿美元的预付款,并可能获得潜在的里程碑和期权付款,以及商业销售的分级特许权使用费,总潜在里程碑价值高达52亿美元。
4.睿健医药宣布完成B+轮融资,本轮融资由北极光创投、创景资本、元希海河等机构共同完成,融资资金将用于加速该公司帕金森病治疗产品NouvNeu001/NouvNeu003,以及眼科治疗产品NouvSight001的临床推进,同时夯实公司早期研发和临床团队建设。
药品集中采购
1.北京市公共资源交易服务平台发布《2025年流感疫苗招标采购项目(非免疫)中标结果公告》。长春生物制品研究所有限责任公司、上海生物制品研究所有限责任公司、华兰生物疫苗股份有限公司等企业的产品中标。
2.上海阳光医药采购网发布3则《关于暂停部分药品采购资格的通知》。因部分企业未按要求调整药品价格,其相关药品采购资格被暂停,包括成都赛诺联创生物科技有限公司的复方醋酸钠林格注射液,信合援生制药股份有限公司、四川美大康佳乐药业有限公司、酒泉大得利制药股份有限公司的复方氨基酸注射液(18AA)等。 (刘鹤整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐